Verteilungskoeffizient
Der Verteilungskoeffizient ist die Gleichgewichtsverteilung eines Analyten zwischen der Probenphase und der Gasphase.
Proben müssen hergestellt werden, um die Konzentration der flüchtigen Bestandteile im Kopfraum zu maximieren und unerwünschte Verunreinigungen von anderen Verbindungen in der Probenmatrix zu minimieren. Um die Konzentration eines Analyten im Kopfraum zu bestimmen, müssen Sie den Verteilungskoeffizienten (K) berechnen.
K-Werte von üblichen Lösungsmitteln in Luft-Wasser-Systemen bei 40 ° C
| Lösungsmittel | Cyclohexane | n-Hexane | Tetrachlorethylene | 1,1,1-Trichlormethane | O-Xylene | Toluene | Benzene | Dichlormethane |
| K-Wert | 0.077 | 0.14 | 1.48 | 1.65 | 2.44 | 2.82 | 2.90 | 5.65 |
| Lösungsmittel | n-Butylacetate | Ethylacetate | Methylethylketone | n-Butanol | Isopropanol | Ethanol | Dioxane | |
| K-Wert | 31.4 | 62.4 | 139.5 | 647 | 825 | 1355 | 1618 |
Berechnung des Verteilungskoeffizienten
Verteilungskoeffizient (K) = Cs / Cg
wobei: Cs ist die Konzentration des Analyten in der Probenphase; Cg ist die Konzentration des Analyten in der Gasphase
Verteilungskoeffizienten von gebräuchlichen Verbindungen
Verbindungen mit niedrigen K-Werten neigen dazu, leichter in die Gasphase zu trennen und haben relativ hohe Reaktionen und niedrige Nachweisgrenzen. Ein Beispiel hierfür wäre Hexan in Wasser: bei 40 ° C würde Hexan in einem Luft-Wasser-System einen K-Wert von 0,14 aufweisen. Verbindungen, die hohe K-Werte aufweisen, neigen dazu, weniger leicht in die Gasphase zu verteilen und haben relativ niedrige Reaktionen und hohe Nachweisgrenzen. Ein Beispiel hierfür wäre Ethanol in Wasser: Ethanol hat bei 40 ° C einen K-Wert von 1355 in einem Luft-Wasser-System.
style="text-align:justify">Die Verteilungskoeffizientenwerte für andere übliche Verbindungen sind in der Tabelle oben dargestellt.Änderung des Partitionskoeffizienten
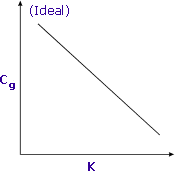 |
Die Empfindlichkeit wird erhöht, wenn K minimiert wird |
Der Verteilungskoeffizient kann auch durch Zugabe von Salzen oder durch ändern des Phasenverhältnisses geändert werden. Diese werden in den nächsten beiden Abschnitten untersucht.
Hinzufügen von anorganischen Salzen
Hohe Salzkonzentrationen in wässrigen Proben verringern die Löslichkeit von polaren organischen flüchtigen Bestandteilen in der Probenmatrix und fördern deren Übertragung in den Kopfraum, was zu niedrigeren K-Werten führt. Die Größe der Aussalzeffekt auf K ist jedoch nicht für alle Verbindungen gleich.
Verbindungen mit K-Werten, die bereits relativ niedrig sind, erfahren eine sehr geringe Änderung des Verteilungskoeffizienten nach Zugabe eines Salzes zu einer wässrigen Probenmatrix.
Im allgemeinen werden flüchtige polare Verbindungen in polaren Matrizen (wässrige Proben) die größten Verschiebungen in K erfahren und haben höhere Reaktionen nach der Zugabe von Salz zur Probenmatrix.
Gebräuchliche Salze zur Verminderung der Matrixeffekte:
- Ammoniumchlorid
- Ammoniumsulfat
- Natriumchlorid
- Natriumcitrat
- Natriumsulfat
- Kaliumcarbonat
Der Wert von K ist auch vom Phasenverhältnis abhängig. Dies wird im nächsten Abschnitt diskutiert.
Phasenverhältnis
Das Phasenverhältnis (β) ist definiert als das relative Volumen des Kopfraums im Vergleich zum Volumen der Probe in der Probenampulle.
|
Berechnung des Phasenverhältnisses Phasenverhältnis (β) = Vg / Vs woher: Vs ist das Volumen der Probenphase |
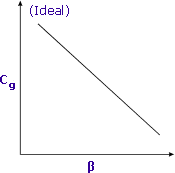 Die Empfindlichkeit wird erhöht, wenn β minimiert wird |
Niedrigere Werte von β (d.h. größere Probengröße) ergeben höhere Antworten für flüchtige Verbindungen.
Eine Verringerung des β-Werts führt nicht immer zu einer Erhöhung der Antwort, die erforderlich ist, um die Empfindlichkeit zu verbessern.
Wenn β durch Erhöhen der Probengröße verringert wird, verteilen Verbindungen mit hohen K-Werten im Vergleich zu Verbindungen mit niedrigen K-Werten weniger in den Headspace und ergeben entsprechend kleinere Änderungen in Cg.
Proben, die Verbindungen mit hohen K-Werten enthalten, müssen optimiert werden, um den niedrigsten K-Wert bereitzustellen, bevor Änderungen im Phasenverhältnis vorgenommen werden.
Kombination von Verteilungskoeffizient und Phasenverhältnis
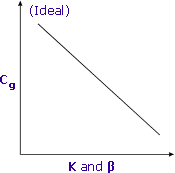
Niedriger K und β führen zu höherem Cg und besserer Empfindlichkeit
Verteilungskoeffizienten und Phasenverhältnisse arbeiten zusammen, um die Endkonzentration von flüchtigen Verbindungen im Kopfraum von Probengefäßen zu bestimmen.
Die Konzentration der flüchtigen Verbindungen in der Gasphase kann wie folgt ausgedrückt werden:
Cg = Co / (K + β)
wobei
Cg ist die Konzentration an flüchtigen Analyten in der Gasphase
und
Co die ursprüngliche Konzentration an flüchtigen Analyten in der Probe ist.
Das Streben nach den niedrigsten Werten für K und β führt zu höheren Konzentrationen an flüchtigen Analyten in der Gasphase und daher zu einer besseren Empfindlichkeit.